Welkom! Je bent uitgekomen op de nieuwe website van Voedingsgeneeskunde. De reguliere website is aan vernieuwing toe. Surf gerust rond, de website is nog niet compleet en volop in ontwikkeling.

Genetische varianten in genen die coderen voor enzymen die belangrijk zijn voor het vetzuurmetabolisme lijken een rol te spelen bij het optreden van ADHD. Deze enzymen, vetzuur-desaturases, zijn betrokken bij het in stand houden van gezonde spiegels van omega-6- en omega-3-lange-keten meervoudig onverzadigde vetzuren (LCPUFA’s). LCPUFA’s spelen een cruciale rol voor de hersenontwikkeling en -functie. Genetische varianten in desaturases zouden mede kunnen verklaren waarom kinderen met ADHD vaak lagere concentraties hebben van omega-3-LCPUFA’s, terwijl de vetzuurinname niet per se anders is dan bij kinderen zonder ADHD.
Suppletie met vetzuren is voornamelijk gericht op het verbeteren van de omega-3-vetzuurstatus. Echter, er zijn aanwijzingen dat ook het omega-6-vetzuur gamma-linoleenzuur geïntegreerd zou moeten worden in de suppletie.
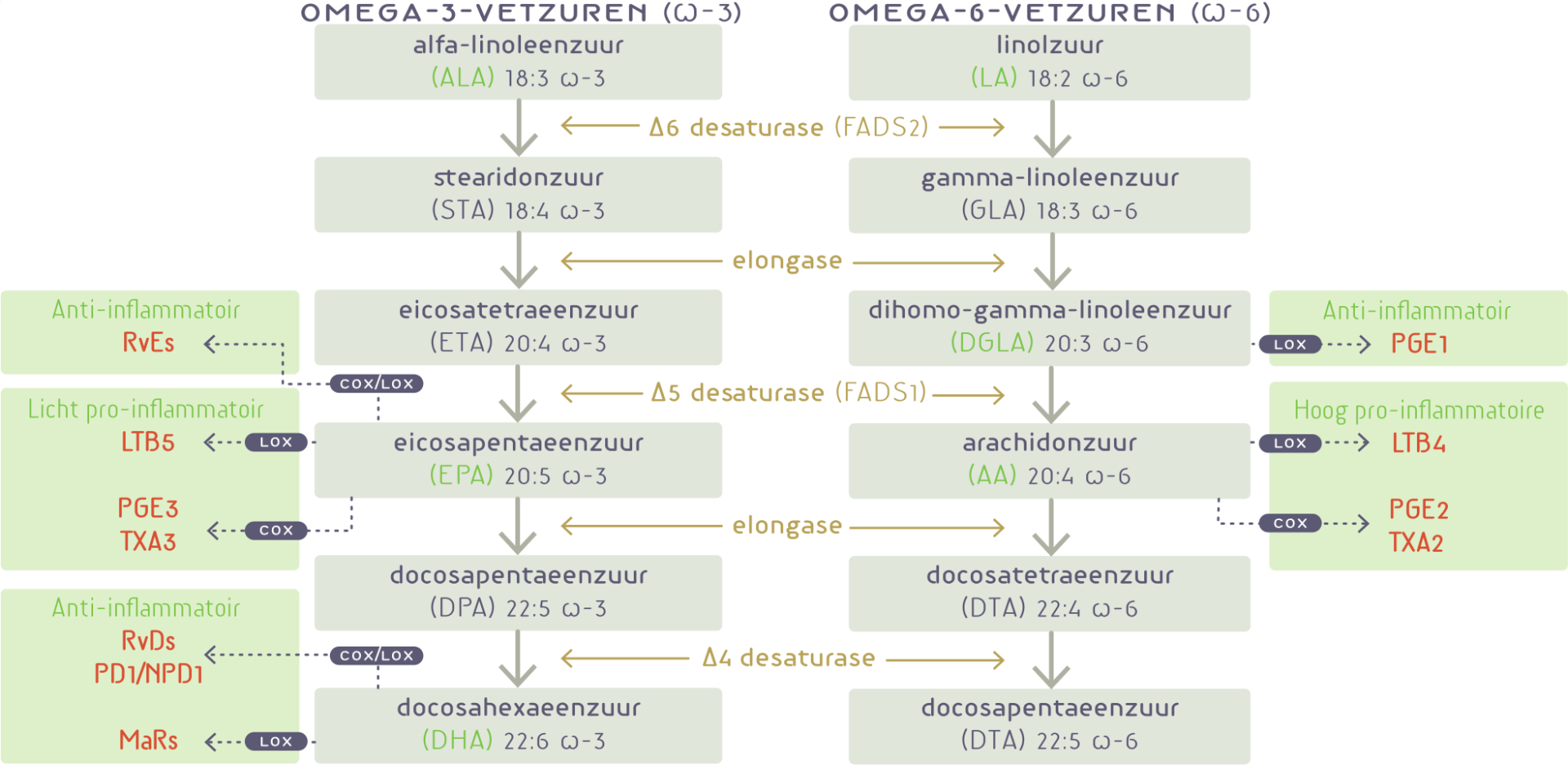
Vetzuurdesaturases zijn enzymen die, samen met elongases, LCPUFA’s vormen uit de essentiële vetzuren linolzuur en alfa-linoleenzuur, zie figuur 1. Daarbij concurreren omega-3-vetzuren met omega-6-vetzuren voor de gemeenschappelijke desaturases en elongases. Bovendien concurreren ze met elkaar bij de incorporatie in celmembranen, waarvan ze een groot deel uitmaken, en hebben ze tegengestelde fysiologische functies.1,2 Het drooggewicht van de hersenen bestaat voor 15-30% uit omega-6- en omega-3-LCPUFA’s2, wat het enorme belang van deze vetzuren laat zien voor de hersenen, met name van arachidonzuur (AA), eicosapentaeenzuur (EPA) en docosahexaeenzuur (DHA).
Genetische varianten in vetzuurdesaturases leiden tot verschillen in individuele vetzuurprofielen in bloedplasma en celmembranen. Genoomwijde associatie studies (GWAS) hebben inmiddels duidelijk gemaakt dat deze genvarianten wijdverspreid en algemeen voorkomen onder de bevolking. Veranderingen in de activiteit van desaturases zijn geassocieerd met metabole en inflammatoire aandoeningen.3 Het is aannemelijk dat dit ook bij ADHD-symptomen een rol speelt.
De actie van delta-6-desaturase is de kritieke en snelheidsbepalende stap voor de vorming van LCPUFA’s. Een verlaagde enzymactiviteit van desaturases resulteert in een gebrekkige productie van omega-6- en omega-3-LCPUFA’s en verstoorde incorporatie van deze vetzuren in celmembranen.4,5 Dit heeft gevolgen voor de structuur en functie van celmembranen, inclusief functies van membraantransporters en -receptoren en functies betrokken bij (dopaminerge) neurotransmissie. Bovendien leidt een veranderde activiteit van desaturases tot een veranderd patroon in de vele vetzuurmetabolieten van LCPUFA’s. Samen leidt dit tot een veranderde cell signaling, wat een invloed heeft op cognitieve functies, gedrag en gemoed en op talloze andere (patho)fysiologische functies waarbij LCPUFA’s en hun metabolieten betrokken zijn.
Van de vele genvarianten (Single-nucleotide Polymorphisms) op het Fatty Acid Desaturase (FADS)-cluster zijn met name FADS1 rs174556 en FADS1 rs174537 (coderend voor delta-5-desaturase) sterk geassocieerd met lagere concentraties van arachidonzuur, EPA en DHA.4,6 FADS1 rs174537 is bovendien geassocieerd met lagere spiegels van GLA.7 De FADS1-variant rs174548 verklaart bijna 30% van de variatie in arachidonspiegels onder de bevolking.6
FADS2 rs498793 (coderend voor delta-6-desaturase) wordt specifiek geassocieerd met ADHD. Verder zijn ook FADS1 rs174545 en rs174548 geassocieerd met ADHD, maar alleen bij kinderen die prenataal blootgesteld zijn aan alcohol.4
Genvariaties van desaturases worden doorgegeven van ouder op kind. Daarnaast beïnvloeden genvarianten vetzuurspiegels in het bloed van zwangere vrouwen en van belangrijke vetzuren in moedermelk tijdens de lactatieperiode.4
In het afgelopen decennium is steeds duidelijker geworden dat een DHA-tekort bij kinderen in relatie staat met hyperactiviteit, leerproblemen, mentale retardatie, epilepsie en autisme. Dit hangt samen met het feit dat een tekort aan DHA de neurotransmissie via dopamine (en serotonine en noradrenaline) verstoort. De verminderde capaciteit om DHA te synthetiseren door de aanwezigheid van bepaalde genvarianten van desaturases, versterken de gevolgen van een te lage inname van omega-3-vetzuren.8
In proefdierstudies is waargenomen dat een chronisch gebrek aan omega-3-vetzuren door generaties heen niet alleen leidt tot een verstoring van het leer- en probleemoplossend vermogen en in het gedrag, maar zorgelijker nog, een ontregeling geeft van de dopamine-afhankelijke neurotransmissie die niet volledig herstelt door suppletie met LCPUFA’s.9,10
Omega-6:omega-3-ratio
DHA, EPA en AA zijn van cruciaal belang voor de architectuur en functie van de hersenen, met name in de latere fase van de zwangerschap en de eerste periode na de geboorte.2 Daarbij heeft de balans tussen deze omega-3- en omega-6-vetzuren een belangrijke invloed op het functioneren van de hersenen. De genetisch bepaalde capaciteit van desaturases, met andere woorden de aanwezigheid van specifieke FADS-varianten, beïnvloedt de omega-6-/omega-3-vetzuurbalans. Verschillen in de hoeveelheden die van deze vetzuren geconsumeerd worden en verschillen in hun affiniteit voor desaturases zijn eveneens bepalend voor de vetzuurbalans.2,11 Daarnaast hebben ook bepaalde ziektes (bijvoorbeeld diabetes), voedingsgewoonten en bepaalde nutriëntentekorten (met name zinktekort) invloed op de activiteit van desaturases.
Geschat wordt dat de omega-6:omega-3-ratio in een westers voedingspatroon op 15:1 tot 20:1 ligt, terwijl een ratio van 1:1 tot 4:1 gezien wordt als een optimale ratio.2 Het nastreven van een lagere omega-6:omega-3-vetzuur ratio vermindert ook de competitie voor desaturases wat ten gunste komt van de vorming van omega-3-LCPUFA’s.12 Dit geldt des te meer in geval er een verminderde activiteit van desaturases in het spel is.
Kinderen met ADHD-symptomen hebben vaak een hogere omega-6:omega-3-ratio dan andere kinderen, zoals blijkt uit verschillende studies, zowel in bloedplasma als in celmembranen.2 Dit is in overeenstemming met de bevinding van een cohortstudie dat een hogere prenatale AA:EPA+DHA-ratio, gemeten in het bloedplasma van de navelstreng, in verband staat met een verhoogde ADHD-index op zevenjarige leeftijd van het kind.2
Verder is gevonden dat een verhoogde omega-6:omega-3-ratio en AA:DHA-ratio in het derde trimester van de zwangerschap geassocieerd zijn met een slechtere motorische ontwikkeling bij het kind.1 In het derde trimester vindt er een groeispurt plaats van de foetale hersenen en is de overdracht van DHA en andere essentiële vetzuren via de navelstreng op zijn hoogst.1 Daarnaast kan een hogere omega-6:omega-3-ratio bij kinderen met ADHD deels toegeschreven worden aan een abnormale verwerking van LCPUFA’s2, zoals bij desaturase en elongase genvarianten en andere genvarianten gerelateerd aan het vetzuurmetabolisme, zoals die betrokken zijn bij vetzuurtransport en -afbraak.
Een studie bij 7-9 jarige kinderen laat zien dat de omega-6/3-vetzuurverhouding een belangrijke factor is voor de cognitieve ontwikkeling (planning van taken, werkgeheugen) en bevestigt het inzicht dat het aandeel van omega-3-vetzuren voldoende groot moet zijn.11
Vetzuursuppletie
Voedingssuppletie met omega-3-vetzuren ter verbetering van de omega-6-/omega-3-vetzuurbalans ligt voor de hand, zeker in geval van FADS-genvarianten. Vetzuursuppletie kan de implicaties omzeilen van een tekort aan omega-3-LCPUFA’s door een verminderde werking van desaturases in combinatie met een langdurig lage inname via de voeding.8,12
Neuro-inflammatie speelt een rol bij ADHD.13 EPA, DHA en GLA (via DGLA) hebben via hun metabolieten ontstekingsremmende effecten. Daarentegen zijn veel metabolieten van AA pro-inflammatoir (zie figuur 1). Een hogere omega-6:omega-3-ratio is pro-inflammatoir. Suppletie met omega-3-vetzuren tijdens kritieke periodes in de zwangerschap en gedurende de eerste postnatale maanden en borstvoeding zou bevorderlijk zijn voor een anti-inflammatoire ‘omgeving’ ten gunste van een gezonde hersenontwikkeling.14 Dit zou nog sterker kunnen gelden voor zwangere vrouwen met ADHD-symptomen. Bij hen zijn een hogere omega-6:omega-3-vetzuurratio en hogere spiegels van de ontstekingscytokine TNF-alfa gevonden (in het derde trimester) dan bij controlepersonen, terwijl hun inname van vetzuren of andere relevante nutriënten niet verschillend was dan die van de controlegroep.15 Dit ondersteunt verder ook het idee dat ADHD-geassocieerde veranderingen in plasmaconcentraties van vetzuren eerder het resultaat zijn van een veranderd vetzuurmetabolisme dan van verschillen in de voedingsinname van deze vetzuren.4,15
Toegevoegde waarde GLA
Desaturases worden gereguleerd door een negatieve terugkoppeling, zodat ze onderdrukt worden bij adequate vetzuurspiegels. Dit houdt in dat wanneer de verhouding waarin omega-6- en omega-3-vetzuren geconsumeerd worden niet in balans is, de overmaat van het ene type vetzuur de omzetting van het andere type vetzuur in LCPUFA’s onderdrukt.4 Een mogelijk gevaar van eenzijdige suppletie met alleen omega-3-vetzuren is daarom dat dit, afhankelijk van de dosis en resulterende omega-6/3-vetzuurverhouding in het lichaam, verlaging van de plasmaconcentraties kan geven van gamma-linoleenzuur (GLA) en dihomo-gamma-linoleenzuur (DGLA) en soms ook van arachidonzuur. Verlaging van deze vetzuren (ook GLA en DGLA hebben fysiologische functies) is ongunstig voor de ontwikkeling van de foetus en het jonge kind.16,17 Een relatief hoge DHA-dosis kan delta-6-desaturase onderdrukken.8 Wanneer omega-3-vetzuren in combinatie worden gegeven met GLA verbetert dit de plasmaspiegels van GLA en DGLA en omega-3-vetzuren, zonder een ongunstig effect op AA-spiegels. Anderzijds ontstaat er door de combinatie van GLA met omega-3-vetzuren ook geen ongewenste toename van AA, zoals wanneer alleen GLA wordt gegeven. EPA remt namelijk het delta-5-desaturase.18
Metabolieten (oxylipinen) van DGLA, zoals PGE1 en 15-HETrE, kunnen samen met die van EPA en DHA tegenwicht bieden aan de meer potente, pro-inflammatoire eicosanoïden van AA, zoals prostaglandine E2 (PGE2) en leukotrieen B4 (LTB4) (zie figuur 1).19 Suppletie met GLA, bijvoorbeeld uit teunisbloemolie of borage-olie, leidt in het lichaam snel tot de vorming van DGLA. Door combinatie met omega-3-vetzuren zal dit geen toename geven van AA en van pro-inflammatoire metabolieten van AA.
Oxylipinen en inflammatie
De vele regulerende functies van omega-6- en omega-3-vetzuren komen grotendeels tot stand via hun metabolieten (oxylipinen). Oxylipinen worden enzymatisch gevormd door cyclo-oxygenases, lipoxygenases, CYP450-enzymen, of door niet-enzymatische auto-oxidatie.17 De best bekende oxylipinen zijn de eicosanoïden (prostaglandinen, tromboxanen, leukotriënen en lipoxinen) van arachidonzuur. Ook de eicosanoïden van EPA en docosanoïden van DHA zijn uitgebreid in kaart gebracht.
Met enkele uitzonderingen zijn de oxylipinen van arachidonzuur potenter dan die van EPA en DHA. Oxylipinen van arachidonzuur spelen een belangrijke rol voor leerfuncties en andere cognitieve functies. Resolvinen afkomstig van EPA en resolvinen, protectinen en maresinen van DHA zijn inflammatie-oplossend en ook van AA zijn inflammatie-oplossende oxylipinen bekend. Pro-inflammatoire oxylipinen van AA hebben een functie voor fysiologische processen, bijvoorbeeld voor immuunfuncties, maar zijn tevens betrokken bij ontregelde pathologische processen.
Ondanks dat een aantal genvarianten van desaturases leiden tot verlaagde spiegels van arachidonzuur, kan de aanmaak van eicosanoïden afkomstig van arachidonzuur juist toenemen onder invloed van deze genvarianten. Zo hebben personen met het FADS genvariant dat het sterkst geassocieerd is met lage arachidonspiegels (FADS1 rs174537), een verhoogde neiging om pro-inflammatoire leukotriënen te produceren, namelijk leukotrieen B4 en 5-HETE.6
Verder werd bij kinderen vastgesteld dat nog weer andere FADS-varianten een verhoogde aanmaak geven van leukotriënen van arachidonzuur (11-HETE) en linolzuur (9-HODE, 13 S-HODE).20 De pro-inflammatoire invloed van FADS-varianten wijst nog eens op het belang van een adequate inname van omega-3-vetzuren (EPA en DHA). Oxylipinen van EPA en DHA hebben neuroprotectieve eigenschappen.21
Combinatie van GLA, EPA en DHA
Voedingssuppletie met een combinatie van GLA, EPA en DHA kan bij een aantal kinderen verbeteringen geven van stemming, sociaal gedrag en cognitieve vermogens (leervermogen, taal en leesvaardigheid), met name bij degenen met een lage omega 3-index en een verhoogde mate van inflammatie.22,23
Uit het vele onderzoek naar het effect van vetzuren bij ADHD komt een combinatie van EPA en DHA met GLA als meest veelbelovend naar voren.24 Daarbij wordt een effect pas goed merkbaar na minstens zes tot acht weken consequent gebruik. Als toevoeging aan de behandeling van ADHD met methylfenidaat kan suppletie met een combinatie van EPA, DHA en GLA het welzijn van de kinderen en aandachtstekort verbeteren.25 Methylfenidaat zou deels werken via stimulering van de afgifte van dopamine in de hersenen. Van de vetzuurcombinatie van EPA, DHA en GLA is aangetoond (in vitro) dat het de overleving van dopamine-producerende hersencellen verbetert.26
Ook bij volwassenen met ADHD kan voedingssuppletie met omega-3/6-vetzuren (EPA, DHA, GLA) nuttig zijn. Verlaagde spiegels van GLA, AA, EPA en DHA bij kinderen met ADHD kunnen persisteren tot in de volwassenheid.21
Tot besluit
De variatie in spiegels van dihomo-gamma-linoleenzuur (DGLA) tussen individuen wordt voor 53% verklaard door FADS genvarianten.27 Dit stemt overeen met de wetenschap dat bij een deel van de bevolking de omzetting van linolzuur (LA) in gamma-linoleenzuur (GLA) moeizamer verloopt. Terwijl GLA snel wordt omgezet in DGLA, is de stap van LA naar GLA snelheidsbepalend en afhankelijk van de capaciteit van delta-6-desaturase.
Tegen deze achtergrond mag verwacht worden dat omega-3-vetzuursupplementen die tevens GLA bevatten een meer gebalanceerd en vollediger anti-inflammatoir potentieel hebben. Dit kan van nut zijn bij aandoeningen waarbij neuro-inflammatie een rol speelt, zoals bij ADHD(-symptomen).
-
Shahabi B, Hernández-Martínez C, Jardí C, et al. Maternal Omega-6/Omega-3 Concentration Ratio During Pregnancy and Infant Neurodevelopment: The ECLIPSES Study. Nutrients. 2025 Jan 2;17(1):170.
-
López-Vicente M, Ribas Fitó N, Vilor-Tejedor N, et al. Prenatal Omega-6:Omega-3 Ratio and Attention Deficit and Hyperactivity Disorder Symptoms. J Pediatr. 2019 Jun;209:204-211.e4.
-
Brown KM, Sharma S, Baker E, et al. Delta-6-desaturase (FADS2) inhibition and omega-3 fatty acids in skeletal muscle protein turnover. Biochem Biophys Rep. 2019 Mar 15;18:100622.
-
Brookes KJ, Chen W, Xu X, et al. Association of fatty acid desaturase genes with attention-deficit/hyperactivity disorder. Biol Psychiatry. 2006 Nov 15;60(10):1053-61.
-
Pei-Chen Chang J. Personalised medicine in child and Adolescent Psychiatry: Focus on omega-3 polyunsaturated fatty acids and ADHD. Brain Behav Immun Health. 2021 Jul 29;16:100310.
-
Hester AG, Murphy RC, Uhlson CJ, et al. Relationship between a common variant in the fatty acid desaturase (FADS) cluster and eicosanoid generation in humans. J Biol Chem. 2014 Aug 8;289(32):22482-9.
-
Metelcová T, Vaňková M, Zamrazilová H, et al. The effect of SNP (rs174537) in FADS1 gene on fatty acid composition in serum lipids. Endocrine Abstracts (2020) 70 AEP372. doi: 10.1530/endoabs.70.AEP372.
-
Majou D. Synthesis of DHA (omega-3 fatty acid): FADS2 gene polymorphisms and regulation by PPARα. OCL. 2021; 28, 43.
-
Bondi CO, Taha AY, Tock JL, et al. Adolescent Behavior and Dopamine Availability Are Uniquely Sensitive to Dietary Omega-3 Fatty Acid Deficiency. Biol Psychiatry. 2013 Jul 25.
-
Transler C, Mitchell S, Eilander A. Could polyunsaturated fatty acids deficiency explain some dysfunctions found in ADHD? Hypotheses from animal research. J Atten Disord. 2013 Jan;17(1):20-8.
-
Sheppard And KW, Cheatham CL. Omega-6 to omega-3 fatty acid ratio and higher-order cognitive functions in 7- to 9-y-olds: a cross-sectional study. Am J Clin Nutr. 2013 Sep;98(3):659-67.
-
D'Helft J, Caccialanza R, Derbyshire E, et al. Relevance of ω-6 GLA Added to ω-3 PUFAs Supplements for ADHD: A Narrative Review. Nutrients. 2022 Aug 10;14(16):3273.
-
Vázquez-González D, Carreón-Trujillo S, Alvarez-Arellano L, et al. A Potential Role for Neuroinflammation in ADHD. Adv Exp Med Biol. 2023;1411:327-356.
-
Rodriguez-Santana Y, Ochoa JJ, Lara-Villoslada F, et al. Cytokine distribution in mothers and breastfed children after omega-3 LCPUFAs supplementation during the last trimester of pregnancy and the lactation period: A randomized, controlled trial. Prostaglandins Leukot Essent Fatty Acids. 2017 Nov;126:32-38.
-
Gustafsson HC, Dunn GA, Mitchell AJ, et al. The association between heightened ADHD symptoms and cytokine and fatty acid concentrations during pregnancy. Front Psychiatry. 2022 Jul 22;13:855265.
-
Geppert J, Demmelmair H, Hornstra G, et al. Co-supplementation of healthy women with fish oil and evening primrose oil increases plasma docosahexaenoic acid, gamma-linolenic acid and dihomo-gamma-linolenic acid levels without reducing arachidonic acid concentrations. Br J Nutr. 2008 Feb;99(2):360-9.
-
Calder PC. Sex Differences in the Plasma Accumulation of Oxylipins in Response to Supplemental n-3 Fatty Acids. J Nutr. 2021 Mar 11;151(3):462-464.
-
Barham JB, Edens MB, Fonteh AN, et al. Addition of eicosapentaenoic acid to gamma-linolenic acid-supplemented diets prevents serum arachidonic acid accumulation in humans. J Nutr. 2000 Aug;130(8):1925-31.
-
Gabbs M, Leng S, Devassy JG, et al. Advances in Our Understanding of Oxylipins Derived from Dietary PUFAs. Adv Nutr. 2015 Sep 15;6(5):513-40.
-
Buckner T, Johnson RK, Vanderlinden LA, et al. Genome-wide analysis of oxylipins and oxylipin profiles in a pediatric population. Front Nutr. 2023 Mar 28;10:1040993.
-
Irmisch G, Richter J, Thome J, et al. Altered serum mono- and polyunsaturated fatty acid levels in adults with ADHD. Atten Defic Hyperact Disord. 2013 Sep;5(3):303-11.
-
Portwood MM. The Role of Dietary Fatty Acids in Children’s Behaviour and Learning. Nutr Health. 2006;18(3):233-47.
-
Johnson M, Fransson G, Östlund S, et al. Omega 3/6 fatty acids for reading in children: a randomized, double-blind, placebo-controlled trial in 9-year-old mainstream schoolchildren in Sweden. J Child Psychol Psychiatry. 2016 Aug 22.
-
Königs A, Kiliaan AJ. Critical appraisal of omega-3 fatty acids in ADHD treatment. Neuropsychiatric Disease and Treatment. 2016 Jul 26;12:1869-82.
-
Barragán E, Breuer D, Döpfner M. Efficacy and safety of omega-3/6 fatty acids in children with ADHD. Journal of Attention Disorders. 2017 Mar;21(5):433-441.
-
Bartl J, Walitza S, Grünblatt E. Enhancement of cell viability after treatment with polyunsaturated fatty acids. Neurosci Lett. 2014 Jan 24;559:56-60.
-
Tintle NL, Pottala JV, Lacey S, et al. A genome-wide association study of saturated, mono- and polyunsaturated red blood cell fatty acids in the Framingham Heart Offspring Study. Prostaglandins Leukot Essent Fatty Acids. 2015 Mar;94:65-72.

